| Россия |
Химически чувствительные полевые транзисторы и биосенсоры на их основе. Кондуктометрические и амперометрические сенсоры
Ответы
Ответы на вопросы
1. "Биоселектор" – это чувствительный элемент биологического происхождения, который обеспечивает селективную реакцию электрохимического сенсора на нужный аналит. Иммобилизованный на электроде или на мембране биоселектор при наличии в контролируемой среде аналита вступает с ним (и только с ним!) в специфическое взаимодействие. Биоселектор подбирают так, чтобы в результате взаимодействия с аналитом возникали (или, наоборот, расходовались) электрохимически активные продукты (ионы, аммиак, перекись водорода, СО2 и т.п.). Изменение их концентрации улавливает чувствительный к ним электрохимический элемент, вырабатывая соответствующий электрический сигнал.
2. Аббревиатура "ХЧПТ" расшифровывается как "химически чувствительный полевой транзистор". При применении в электрохимических сенсорах он обеспечивает следующие преимущества: малые габариты и энергопотребление, высокую чувствительность, возможность формирования на том же кристалле кремния также всех электронных схем, необходимых для обработки полученных сигналов, относительно небольшая цена и малый требуемый объем пробы.
3. Аббревиатура "ИСПТ" расшифровывается как "ионоселективный полевой транзистор". Это ХЧПТ, у которого чувствительная мембрана модифицирована так, чтобы резко повысить его селективность по отношению к определенному виду ионов.
4. "Биоселективный полевой транзистор" – это ХЧПТ, на затворе которого иммобилизован чувствительный элемент биологического происхождения, обеспечивающий селективную реакцию транзистора на нужный аналит.
5. "Кондуктометрическими" называют электрохимические сенсоры, у которых при изменении концентрации, заряда или состава ионов в исследуемом растворе соответственно изменяется его электропроводность. Т.е. первичные информационные сигналы возникают в виде изменения электропроводности чувствительного элемента.
6. "Импедансными" называют электрохимические сенсоры, у которых при изменении концентрации, заряда или состава ионов в исследуемом растворе соответственно изменяются не только активная, но и реактивная составляющие его электропроводности. Т.е. первичные информационные сигналы возникают в виде изменения импеданса чувствительного элемента.
7. Промышленностью в основном выпускаются кондуктометры для контроля качества питьевой, натуральной, дистиллированной и бидистиллированной, деионизованной воды, для определения общей минерализации технических и минеральных вод, для проверки качества обессоливания морской воды и подобных целей, когда селективность сенсора к какому-то определенному виду ионов не столь важна.
8. "Амперометрическими" называют электрохимические сенсоры, у которых при изменении концентрации, заряда или состава ионов в исследуемом растворе соответственно изменяется ток через электрохимический элемент.
9. "Кулонометрическими" называют электрохимические сенсоры, у которых при изменении концентрации, заряда или состава ионов в исследуемом растворе изменяется величина электрического заряда, перенесенного через электрохимический элемент за какое-то фиксированное время.
10. В амперометрических электрохимических сенсорах сигнал линейно зависит от концентрации ионов в исследуемом растворе, а в потенциометрических – линейно зависит от логарифма концентрации. Поэтому амперометрические сенсоры позволяют точнее измерять концентрацию в рабочем диапазоне. Однако сам рабочий диапазон измерения концентрации у них гораздо уже. В этом они существенно уступают потенциометрическим сенсорам.
11. Фермент "глюкозооксидазу" в качестве биоселектора применяют в амперометрических сенсорах для измерения небольших концентраций глюкозы, в первую очередь, для измерения концентрации глюкозы в крови человека.
12. "Тестовые полоски" в амперометрических и кулонометрических сенсорах для измерения сахара крови представляют собой специально изготовленную часть электрохимической ячейки. В их активной области, которая вставляется между электродами сенсора, иммобилизованы глюкозооксидаза и резервы кислорода. Предусмотрены пути капиллярного всасывания в эту активную область необходимого для измерения объема исследуемой крови. На тестовой полоске сформированы также вспомогательные элементы – для автоматического включения питания глюкометра при вставленной полоске, для считывания условного кода полоски и т.д.
Ответы к упражнениям
Упражнение 16.1. Функциональная схема электрохимического биосенсора имеет следующий вид:
Биоселектор подбирают так, чтобы в результате взаимодействия с аналитом возникали (или, наоборот, расходовались) электрохимически активные продукты (ионы, аммиак, перекись водорода,  и т.п.). Иммобилизованный (т.е. осажденный и закрепленный) на электроде или на мембране биоселектор при наличии в контролируемой среде аналита вступает с ним (и только с ним!) в специфическое взаимодействие. Изменение концентрации продуктов такого взаимодействия чутко улавливает чувствительный к ним электрохимический элемент, вырабатывая соответствующий электрический сигнал. Этот сигнал усиливается и обрабатывается в электронном блоке, который и выдает на выход информацию о результатах обнаружения и измерения.
и т.п.). Иммобилизованный (т.е. осажденный и закрепленный) на электроде или на мембране биоселектор при наличии в контролируемой среде аналита вступает с ним (и только с ним!) в специфическое взаимодействие. Изменение концентрации продуктов такого взаимодействия чутко улавливает чувствительный к ним электрохимический элемент, вырабатывая соответствующий электрический сигнал. Этот сигнал усиливается и обрабатывается в электронном блоке, который и выдает на выход информацию о результатах обнаружения и измерения.
Вариант 1. Биоселектором могут быть фермент, нуклеиновая кислота, антитело, живая клетка, готовый живой рецептор и другие биологические структуры, которые могут обеспечить селективную реакцию на нужный аналит. В результате взаимодействия с аналитом должны возникать (или, наоборот, расходоваться) электрохимически активные продукты (ионы, перекись водорода, аммиак и т.п.).
Вариант 2. Живые клетки растений, животных и особенно микроорганизмов легко доступны, могут культивироваться и воссоздаваться в чистой культуре. В отличие, например, от ферментов здесь не нужны значительные затраты на выделение и очищение. Для многих видов клеток разработаны эффективные методы генетических манипуляций, позволяющие получать мутанты с высоким содержанием того или иного фермента либо белка. Особенности метаболизма клеток позволяют подбирать клетки, как избирательно чувствительные к отдельным видам молекул, так и ориентированные на довольно широкие классы химических веществ (даже, например, на весь класс веществ, пригодных для биологического усвоения). Разработанные методы иммобилизации живых клеток позволяют поддерживать их жизнеспособность и активность в течение нескольких лет. Преимущества живых клеток в качестве биоселекторов можно сочетать с преимуществами химически чувствительных полевых транзисторов.
Вариант 3. Одним из наиболее известных примеров применения в качестве биоселектора одного из природных ферментов является применение глюкозооксидазы в амперометрических и кулонометрических сенсорах глюкозы. Глюкозооксидаза – это доступный, недорогой фермент, который добывают из Aspergillus niger и который долго сохраняет свои свойства. Благодаря этому удалось создать и выпускать промышленно наборы одноразовых электрохимических "полосок" для анализов крови на глюкозу с гарантированным сроком использования до 1 года. Глюкозооксидаза очень избирательно вступает во взаимодействие именно с молекулами глюкозы и способствует их окислению. В процессе окисления происходит перенос электрического заряда через электрохимическую ячейку, что и позволяет косвенно определять концентрацию глюкозы в исследуемом растворе.
Вариант 4. Одним из примеров применения в качестве биоселектора готового живого рецептора может служить использование для создания "электронного носа" естественных обонятельных рецепторов человека НР 1740. В работе [
[
174
]
] показано, что в электрохимическом импедансном сенсоре с таким рецептором путем измерения его импеданса на разных частотах удается надежно обнаруживать присутствие специфического лиганда "альдегид Helional  " в концентрациях меньше 10–10 моль. Продемонстрирована и высокая селективность биосенсора с таким рецептором: внесение похожего, но не специфического лиганда – гептаналя – в тех же условиях не приводило к изменениям импеданса.
" в концентрациях меньше 10–10 моль. Продемонстрирована и высокая селективность биосенсора с таким рецептором: внесение похожего, но не специфического лиганда – гептаналя – в тех же условиях не приводило к изменениям импеданса.
Упражнение 16.2.
Вариант 1. При измерении электропроводности на постоянном токе возникают проблемы, связанные с электродными потенциалами, с появлением и перезарядкой двойного электрического слоя на границах раздела "электронный проводник - ионный проводник", а также с явлениями электролиза. При измерениях в режиме переменного тока на электродах периодически происходит быстрое изменение поляризации, и благодаря этому течет стационарный переменный ток. Измеряется так называемый "адмитанс" – модуль комплексного числа, действительной частью которого является омическая проводимость, а мнимой – емкостная проводимость электрохимической ячейки. Частотная зависимость адмитанса может давать дополнительную ценную информацию о составе контролируемого раствора.
Вариант 2. Кондуктометрические биосенсоры используют для определения концентрации ряда важных веществ, например, мочевины и ацетилхолина. Разработаны кондуктометрические биосенсоры, способные зарегистрировать даже незначительные загрязнения воды антибиотиками, фосфорорганическими пестицидами, гипохлоритом, цианидами и т.д. Их применяют для контроля за биотехнологическими процессами, в экологии, в фармакологии. Описан, например, кондуктометрический электрохимический биосенсор на основе иммобилизованных холинестераз для определения концентраций фосфорорганических и карбаматных пестицидов, гипохлорита, общей токсичности воды, а также гликоалкалоидов – нежелательных натуральных токсических веществ, иногда содержащихся в картофеле, в томатах и в баклажанах.
Вариант 3. Импедансные газовые сенсоры на основе окислов и нитридов металлов, механизм действия которых раньше связывали только с физической абсорбцией молекул газов, на самом деле оказались сложнее. Абсорбция молекулы газа, особенно химически активного, почти всегда сопровождается его электрохимическим взаимодействием с полупроводником. Это – разрыв одних и образование новых слабых связей, изменение зарядового состояния примесных и поверхностных энергетических уровней, нередко даже ионизация атомов, перенос электрического заряда через поверхность кристаллических зерен. Отличие от классических электрохимических сенсоров состоит только в том, что указанные взаимодействия происходят не непосредственно возле электродов, а на поверхностях раздела кристаллических зерен. Всё это и дает основание отнести полупроводниковые газовые сенсоры к классу электрохимических.
Вариант 4. После адсорбции молекул газа, электрохимических взаимодействий и установления пусть и слабых химических связей с ними, молекулы газа при обычных температурах остаются достаточно прочно связанными. Для того, чтобы импедансный полупроводниковый газовый сенсор стал пригодным к новым измерениям, надо удалить с его поверхности уже адсорбированные молекулы газов. Именно с этой целью в конструкцию сенсоров обязательно вводят тонкоплёночные нагреватели. При нагревании поверхности сенсора до температуры, при которой относительно слабые временные связи разрываются, и происходит десорбция молекул газа. Нагреватели создают также возможность повышения селективности сенсора. Дело в том, что чувствительность сенсора к разным газам с ростом температуры изменяется по-разному. Эта зависимость всегда имеет вид кривой с максимумом. Поэтому, изменяя с помощью пленочного микронагревателя температуру окисла и измеряя импеданс при разных температурах, можно вычленить влияние разных газов, "узнавать" и различать их.
Упражнение 16.3.
Вариант 1. Ионы, которые находятся вблизи электрода, после подачи на электрохимический элемент постоянного внешнего напряжения сразу вступают в химическую реакцию, их концентрация здесь быстро уменьшается и становится значительно ниже, чем в основном объеме электролита. Из-за уменьшения концентрации ионов снижается скорость реакции и уменьшается обусловленный ею электрический ток (поток электрических зарядов). Возникает градиент концентрации, который стимулирует диффузию ионов из объема к электроду. К этому добавляется также дрейф ионов под действием слабого электрического поля, возникающего в электролите. Со временем устанавливается новое динамическое равновесие, когда количество ионов, вступающих за единицу времени в химические реакции возле электродов, сравнивается с количеством ионов, которые подходят к электродам из объема электролита посредством диффузии и дрейфа. При выполнении этого условия электрический ток перестает изменяться.
Вариант 2. "Кислородный электрод Кларка" устроен следующим образом. В пластмассовом цилиндрическом корпусе сделаны сквозные отверстия для проводников, в которых размещены индикаторный (рабочий) электрод из платины и электрод сравнения из серебряных проволок, концы которых покрыты пастой из хлорида серебра. Нижний конец корпуса обтягивают газопроницаемой полимерной мембраной из полипропилена (полиэтилена, фторопласта, целлофана и т.п.). В пространство между электродами и мембраной залит водный раствор хлорида кальция. Извне мембрана контактирует с контролируемой средой – газом или жидкостью. Если в контролируемой среде кислорода нет, то при подаче напряжения между электродом сравнения (анод) и рабочим электродом установившийся стационарный ток очень слаб. Если же в контролируемой среде кислород имеется, то его молекулы диффундируют сквозь мембрану и через раствор хлорида кальция. Когда они достигают платинового электрода, то благодаря каталитическим свойствам платины здесь кислород соединяется с ионами водорода с образованием воды. Вследствие этого ток через электрохимический элемент значительно возрастает. Стационарный ток линейно зависит от концентрации кислорода в контролируемой среде.
Вариант 3. На рабочую зону тестовой полоски нанесен полиакриламидный гель с иммобилизованной в нем глюкозооксидазой. Когда тестовая полоска вставлена в сенсор, её рабочая зона электрически контактирует с электродами. Капелька крови пациента всасывается капиллярными силами в рабочую зону. Имеющиеся в ней молекулы глюкозы притягиваются к глюкозооксидазе и вступают в ферментативную химическую реакцию с имеющимися в тестовой полоске молекулами кислорода. Поскольку молекул кислорода вполне достаточно, то скорость реакции и текущий через электрохимическую ячейку ток пропорциональны концентрации молекул глюкозы в исследуемой крови. Еще на заводе сенсор калибруют, т.е. устанавливают соответствие протекающего тока и концентрации глюкозы.
Вариант 4. В амперометрических сенсорах измеряется величина тока, протекающего через электрохимический элемент, а в кулонометрических сенсорах – общий электрический заряд, протекший через этот элемент. Измеряемый ток может несколько меняться со временем по разным причинам (переходные процессы в электролите, шумы, помехи). При измерении суммарного заряда влияние всех этих причин существенно уменьшается. В этом и состоит преимущество кулонометрических сенсоров.
Упражнение 16.4.
Вариант 1. В одном моле содержится  молекул глюкозы. Если в измерительную электрохимическую ячейку всасывается
молекул глюкозы. Если в измерительную электрохимическую ячейку всасывается  крови с концентрацией глюкозы с ммоль/л, то в ячейку попадает молей глюкозы, т.е. молекул глюкозы. В результате их ферментативного окисления в присутствии глюкозооксидазы через ячейку переносится электрический заряд
крови с концентрацией глюкозы с ммоль/л, то в ячейку попадает молей глюкозы, т.е. молекул глюкозы. В результате их ферментативного окисления в присутствии глюкозооксидазы через ячейку переносится электрический заряд

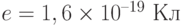 – электрический заряд электрона. Подставляя в эту формулу данные задачи, находим:
– электрический заряд электрона. Подставляя в эту формулу данные задачи, находим: 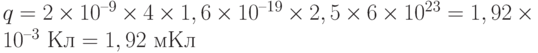 .
.Вариант 2. Из формулы, выведенной в "Варианте 1", находим:  . Подставляя в эту формулу данные задачи, получаем:
. Подставляя в эту формулу данные задачи, получаем:  .
.
Вариант 3. Из формулы, выведенной в "Варианте 1", находим:  . Подставляя в эту формулу данные задачи, получаем:
. Подставляя в эту формулу данные задачи, получаем:  .
.
Вариант 4. 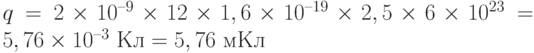 .
.
Вариант 5. 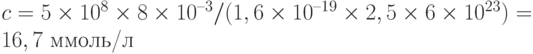 .
.


